У цій статті блогу вільних льодорубом мова піде про природу танення льоду. Чому лід тане, яким чином, за яких умов і з якою швидкістю?
Як відомо, вода в навколишньому середовищі знаходиться в трьох іпостасях - у вигляді рідини, у вигляді пари, і у вигляді твердого тіла (інакше кажучи, льоду), при цьому вода може вільно переходити з твердого агрегатного стану в рідке, з рідкого в газоподібний , і навпаки, завжди повертаючись до вихідних властивостям.
Нуль градусів за шкалою Цельсія (0 ° С), за умови нормального атмосферного тиску в 1 атмосферу (760 мм ртутного стовпа), є температурним значенням фазового переходу води з рідкого стану в тверде (кристали льоду) і, навпаки, з твердого в рідкий. Виходить, що при постійній нульовій температурі вода може бути як льодом, так і рідиною, а питання кристалізації або танення полягає лише в тому, в який початковій фазі складається вода і яке на неї впливають. У цій температурної точці лід продовжує залишатися льодом, а рідина - рідиною, якщо, відповідно, температура навколишнього повітря не підніметься вище нульової позначки або не опуститься нижче неї. В іншому випадку відбувається теплообмін. Тобто, нагрівання льоду при нулі градусів призводить до того, що його температура вже не підвищується - витрачений тепло йде на руйнування кристалічної структури льоду, а після того, як весь лід розтане і стане рідиною, подальше нагрівання зумовить підвищення температури води. В процесі замерзання справа йде рівно навпаки - зі зниженням навколишньої температури нижче нуля вода кристалізується, вивільняючи при цьому кількість енергії (тепла), яке необхідно для танення того ж обсягу льоду.
 Питома теплота плавлення льоду досить висока і дорівнює 335 кДж / кг (кілоджоулів / кілограм); якщо порівняти з іншими речовинами, то у свинцю, наприклад, вона становить лише 25 кДж / кг, у золота - 66.2, у срібла - 105, у заліза - 277. Щоб було більш зрозуміло, скажімо, що для перетворення 1 кг снігу або льоду в воду, потрібно стільки ж енергії, скільки необхідно для нагрівання 1 літра води до температури 80 ° С. Тому, не варто дивуватися тому, що з настанням весни в затінених ділянках підлягає може лежати і не танути сніг. Якби лід мав низьку питому теплоту плавлення, він танув б ще швидше звичайного, а вода в річках і водоймах замерзала б з настанням заморозків.
Питома теплота плавлення льоду досить висока і дорівнює 335 кДж / кг (кілоджоулів / кілограм); якщо порівняти з іншими речовинами, то у свинцю, наприклад, вона становить лише 25 кДж / кг, у золота - 66.2, у срібла - 105, у заліза - 277. Щоб було більш зрозуміло, скажімо, що для перетворення 1 кг снігу або льоду в воду, потрібно стільки ж енергії, скільки необхідно для нагрівання 1 літра води до температури 80 ° С. Тому, не варто дивуватися тому, що з настанням весни в затінених ділянках підлягає може лежати і не танути сніг. Якби лід мав низьку питому теплоту плавлення, він танув б ще швидше звичайного, а вода в річках і водоймах замерзала б з настанням заморозків.
Говорячи про танення льоду або кристалізації рідкої води, варто врахувати деякі істотні фактори, що впливають на ці процеси.
Як було вже зазначено, і для першого, і для другого фазового переходу важливою умовою є тиск. Для більшості речовин характерно те, що при фазовому переході збільшення тиску сприяє збільшенню температури нагрівання. Високий тиск призводить до того, що атоми речовини починають ущільнюватися, відповідно кристалічна решітка стискається, отже, на її руйнування потрібно більше енергії. Однак у випадку з водою залежність температури від тиску виглядає інакше. Вода, замерзаючи, перетворюється в тверде тіло (лід), але на відміну від багатьох речовин, при затвердінні вона не зменшується, а, навпаки, збільшується в об'ємі приблизно на 9%. Щільність льоду менше щільності води в рідкому вигляді, при 0 ° С у льоду вона становить 916.7 кг / м3, а у води - 999.8 кг / м3 (ось чому лід і не тоне у воді), а значить, збільшення тиску сприяє прискоренню переходу води з твердого стану в рідке, що в свою чергу призводить до зниження температури плавлення льоду. Наприклад, щоб знизити температуру плавлення льоду на 1 ° С потрібно збільшити тиск більш ніж на 100 кгс / см2 (кілограм-сила / кв.см) або 10 МПа (мегапаскалей).
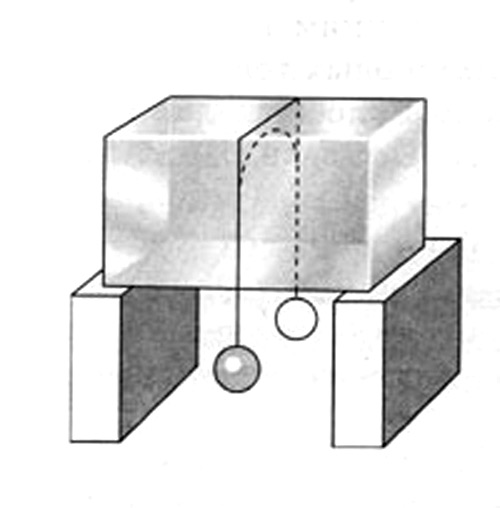
Залежність температури плавлення льоду від тиску
Наочно залежність температури плавлення льоду від тиску можна побачити на досвіді. Через крижаний блок перекидається нейлонова нитка, а до кінців нитки прив'язуються вантажі; під тиском нитки лід тане, нитка опускається, а що утворилася вода слідом за ниткою назад замерзає. Таким чином, нитка поступово проходить крізь лід, а сам крижаний блок в той же час залишається цілим.
Важливою умовою для утворення льоду є вміст у воді найдрібніших суспензій, які будуть в даному випадку бути ядрами крижаних кристалів (про формування крижаних кристалів Ви також можете прочитати в статті « Мікроледяние скульптури »).
Дистильована ж вода, очищена від усяких домішок, може залишатися рідиною і при мінусовій температурі, так як молекулам води не буде за що зачепитися, щоб створити кристалічну решітку, але тільки в тому випадку, коли на воду не впливають. А якщо ж, наприклад, в посудину з очищеною водою кинути шматок льоду або пляшку з дистилятом струсити, процес кристалізації буде миттєвим, і за кілька секунд вода перетвориться на лід, завдяки бульбашок повітря, микрочастицам, що потрапили у воду, нерівностей на поверхні судини.
Дистильована вода перебуваючи на великих висотах у вигляді дрібних крапельок не замерзає навіть при дуже низьких температурах, від -30 ° С і нижче.
На фазові переходи води впливає також ступінь її солоності. Морська вода, на відміну від прісної, замерзає завжди при температурі нижче 0 ° С. Різниця температур її замерзання залежить від концентрації в ній солей, наприклад, при 20% -ної солоності температура замерзання складає близько -1 ° С, а при 40% -ної - трохи вище 2 ° С.
Концентрація солі знижує і температуру плавлення льоду. Ми часто з вами бачили, як заледенілі проїжджі частини і пішохідні доріжки посипали сіллю. Так ось, сіль з'єднуючись з крупинками верхнього шару льоду, завдяки механічній дії, чиниться нашими ногами і колесами автотранспорту, а також сонячних променів і вітру, що викликає подтаіваніе крижаної кірки, утворює свого роду суміш. Температура плавлення сумішей завжди нижче, ніж температура плавлення окремих речовин, тому лід на дорогах починає танути негайно. При таненні утворюється солоний водний розчин, який допомагає розтопити лід далі.
Танення льоду є важливим фактором, що впливає на процес терморегуляції в природі. Однак, втручання людини в природу, забруднення навколишнього середовища і, як наслідок, глобальне потепління, особливо за останні десятиліття, призвело до того, що морський арктичний лід, антарктичний і материковий лід (льодовики) стрімко тануть. Активне танення льоду в свою чергу скорочує ареал проживання полярних тварин, підвищує рівень світового океану, призводить до дисбалансу парникових газів і зміни клімату на планеті в цілому, загрожує життю тварин і людей - в результаті коло замикається (проблема зміни клімату відображена в акції « крижаний ведмідь », Про яку Ви можете прочитати в статті« Крижаний ведмідь »). Зникнення льоду - одна з найгостріших проблем, яку потрібно постаратися вирішити світовій спільноті в найближчі роки.



